來源: 點擊:1681 喜歡:0
2016-11-08 13:51:20 來源: 點擊:
1 引言在酸性環境下, 氧化亞鐵硫桿菌(A.ferrooxidans)可將Fe2+和還原態S分別氧化為Fe3+和SO42-, 同時獲得生命活動中所需要的能量來固定空氣中的CO2和維持自身生長, 在環境工程領域有著廣闊的應用前景.目前, A.ferrooxidans氧化Fe2+和還原態S的特性已經被成功地應用于生物濕法冶金、AMD的治理、煙氣脫硫、煤炭脫硫, 以及污泥、底泥等處理中.
A.ferrooxidans氧化Fe2+的過程通常發生在低pH、富含Fe3+、SO42-及一價陽離子等(如K+、Na+、NH4+等)極端酸性環境中, 通常伴隨有次生羥基硫酸鐵礦物如黃鐵礬、施氏礦物等的生成.黃鐵礬具有不溶解于稀酸, 易于沉淀、洗滌和過濾等優點, 因而被廣泛用于金屬冶煉工業中除鐵.同時, 黃鐵礬也是性能優異、稀有昂貴的赭黃色無機顏料, 且黃鐵礬在作為固定化載體時有助于A.ferrooxidans生物膜的形成.然而, 在實際工程應用中, 黃鐵礬的出現也會帶來負面作用.如煙氣脫硫中, 黃鐵礬的生成會減少反應器中作為氧化劑的Fe3+的濃度;黃鐵礬在管道、閥門等位置的沉積還會影響反應器的正常運轉(Jensen et al., 2005;周順桂等.而另一種次生礦物—施氏礦物, 具有納米級粒度和不規則孔道結構, 比表面積多在100~200 m2·g-1, 且富含羥基、硫酸根等基團, 對重(類)金屬具有很強的吸附能力和共沉淀作用, 在重金屬廢水處理領域具有潛在的應用價值.但若以A.ferrooxidans為主要功能菌的生物酸化來去除污泥或土壤體系固相中的重金屬時, 產生的施氏礦物反而會起到副作用.
可見, 黃鐵礬或施氏礦物都有各自的優缺點, 結合上述實際應用中出現的諸多問題, 本研究主要考察黃鐵礬或施氏礦物的形成條件, 根據實際需求來調整最佳的工藝參數, 進而避免負效應的產生.溫度和pH是容易調控的兩個主要因素, 本試驗擬在A.ferrooxidans改良9K液體培養基體系下, 通過調節反應溫度和初始pH來考察二者對次生產物的綜合影響, 以期為環境治理中有效調控次生礦物的形成提供科學依據.
2 材料與方法
2.1 供試材料
改良9K液體培養基:(NH4)2SO4 3.5 g, KCl 0.119 g, K2HPO4 0.058 g, Ca(NO3)2·4H2O 0.0168 g, MgSO4·7H2O 0.583 g, 蒸餾水1000 mL, pH=2.5, 121 ℃滅菌30 min.
A.ferrooxidans休止細胞制備:將A.ferrooxidans接種在改良9K培養基中, 置于28 ℃、180 r·min-1搖床中振蕩培養, 指數生長階段后期停止培養(約2~3 d).隨后將培養液經定性濾紙過濾以除去生成的鐵沉淀物, 將濾液以10000×g的相對離心力(4 ℃、10 min)離心收集菌體, 并用pH=1.5的酸水(H2SO4配制)洗3次, 除去各種雜離子.將這些菌體懸浮于pH=2.5的酸水(H2SO4配制), 所得即為A.ferrooxidans濃縮菌液.
2.2 試驗設置
在一系列500 mL三角瓶中加入改良9K液體培養基, 按8960 mg·L-1的Fe2+濃度加入FeSO4·7H2O, 用1:1的H2SO4調上述所有體系pH至1.5、2.0、2.5和3.0, 隨后接種A.ferrooxidans休止細胞懸浮液, 并補充去離子水, 使體系的有效容積為250 mL, A.ferrooxidans密度為5×107 cells·mL-1.上述三角瓶分別置于8、18、28和38 ℃搖床中振蕩培養72 h.培養過程中, 定期取液體樣約1 mL過0.22 μm濾膜(取樣前使三角瓶預先靜置5 min, 使次生礦物完全沉降, 然后取上清液), 測定和計算Fe2+濃度、Fe2+平均氧化速度、總Fe沉淀率的變化情況.培養期間采用稱重法定時補加因蒸發減少的水分.培養終點時, 用中速定性濾紙收集合成的次生礦物, 用去離子水清洗2次以去除雜質, 60 ℃烘干后稱重并進行礦物相鑒定.不同處理均設置3個重復.Fe2+氧化率(R1)、總Fe沉淀率(R2)和Fe2+平均氧化速度(V, mg·L-1·h-1)計算公式如下:
(1)
(2)
(3)
式中, [TFe]為總Fe濃度(mg·L-1);X1和X2分別為t1和t2時刻的Fe2+濃度(mg·L-1).
2.3 測定方法
采用pHS-3C精密pH計測定溶液pH值;Fe2+和總Fe濃度采用鄰啡羅啉比色法測定;礦物質量用電子天平稱量;礦物顏色用標準比色卡進行比對;礦物相采用X射線衍射儀測定(XRD, Bruker D8), 測試工作條件為:管電壓40 kV, 管電流40 mA, 掃描區間10°~80°(2θ), 步長0.01°, 掃描速率6°·min-1, Cu靶.
3 結果與討論
3.1 溶液溫度和pH對Fe2+生物氧化的影響
在A.ferrooxidans接種密度為5×107 cells·mL-1, Fe2+濃度為8960 mg·L-1的9K培養基中, 通過改變起始pH和培養溫度來觀察二者對Fe2+氧化、Fe3+水解沉淀及次生礦物形成的綜合影響.圖 1是反應過程中不同處理體系Fe2+的生物氧化情況.另外, 通過計算Fe2+的平均氧化速度來對各處理中Fe2+的氧化速度進行定量比較, 結果如表 1所示.
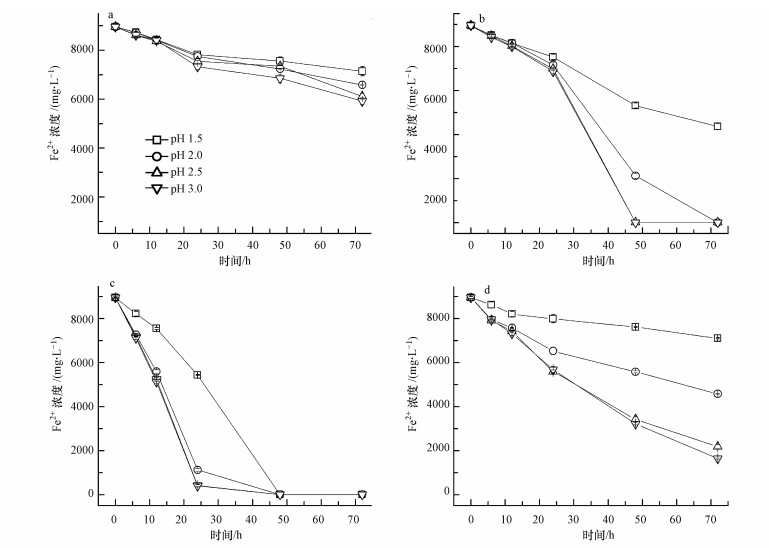
圖 1溶液起始pH和反應溫度對Fe2+氧化的影響(a.8 ℃;b.18 ℃;c.28 ℃;d.38 ℃)
表 1 溶液起始pH和反應溫度對Fe2+平均氧化速度的影響
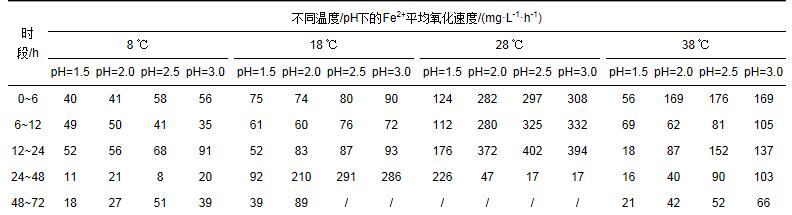
結合圖 1c和表 1可以看出, 28 ℃時A.ferrooxidans氧化Fe2+的速度最快, 這與Daoud 等(2006)的研究結果是接近的.當培養溫度為28 ℃時, 起始pH=2.0~3.0處理中的反應最快, Fe2+的最高平均氧化速度高達402 mg·L-1·h-1(pH=2.5, 12~24 h), 反應至24 h時90%以上的Fe2+被氧化;當pH降到1.5時, Fe2+的氧化速度明顯下降, Fe2+的最高平均氧化速度為226 mg·L-1·h-1(24~48 h), 反應至24 h時Fe2+氧化率只有39.35%.不過, 所有處理的Fe2+都在48 h內被完全氧化.由于A.ferrooxidans在氧化Fe2+的過程中可以獲得自身生命活動所需的能量, 因而在9K培養基中培養時, A.ferrooxidans會不斷繁殖, 菌密度會不斷增加.而因受低pH的影響, A.ferrooxidans活性或繁殖受到抑制, 表現出較低的Fe2+氧化速度.因此, 在圖 1c中可以看到, 在pH 2.0~3.0時, 12~24 h時段Fe2+的平均氧化速度要高于0~12 h時Fe2+的平均氧化速度, 而pH=1.5處理則表現出Fe2+最高氧化速度的延后性.
當溫度升高到38 ℃時, Fe2+的氧化速度明顯變慢, 最高Fe2+平均氧化速率也只有176 mg·L-1·h-1(0~6 h), 此時起始pH=2.5, 反應72 h時只有75.69%的Fe2+被氧化, pH=3.0處理與其相當.此外, 結合圖 1d和表 1可以發現, pH=2.0~3.0時Fe2+的最高平均氧化速度體現在反應初始階段, 其不僅沒有隨著反應時間的延長逐漸提高, 反而表現出明顯下降的趨勢.說明高溫不僅使得A.ferrooxidans的氧化活性受到了抑制, 而且其繁殖能力也受到了影響.尤其是pH=1.5的處理, 高溫加上低pH的雙重影響, A.ferrooxidans一直表現出較低Fe2+氧化速度, 反應72 h時Fe2+累積氧化率只有20.67%.
當溫度為18 ℃時, Fe2+的氧化速度要慢于28 ℃, 但要快于38 ℃.pH越低, 完全氧化Fe2+所需的時間越長, 其中, 起始pH=2.5~3.0處理中的Fe2+在48 h內被完全氧化, pH=2.0處理中的Fe2+被完全氧化則需72 h, pH=1.5處理在72 h反應時間內Fe2+氧化率只有51.26%(圖 1b).對照28 ℃處理可知, 因受溫度的影響, A.ferrooxidans的氧化活性和繁殖能力都迅速下降, 各處理Fe2+的平均氧化速率在0~24 h內都只在52~93 mg·L-1·h-1間起伏, 最高平均氧化速度相對滯后12~24 h.
當溫度只有8 ℃時, 所有處理中Fe2+的氧化速度都很慢, 反應72 h時, Fe2+最高氧化率只有34.02%, 不同處理之間差異較小, 說明相對于pH而言, 溫度對A.ferrooxidans的影響作用更明顯.另外, 表 1中也沒有觀察到Fe2+加速氧化的現象, 不同時段Fe2+平均氧化速度基本在40~90 mg·L-1·h-1之間, 說明8 ℃下不利于A.ferrooxidans的生長繁殖.
3.2 溶液溫度和pH對Fe3+水解成礦的影響
圖 2描述的是在不同的起始pH和反應溫度條件下, 各處理中總Fe沉淀率的變化趨勢.其實質是在一定的pH和溫度、充分的SO42-和一價陽離子(K+、NH4+)體系中, 溶液中的可溶性Fe3+通過水解形成次生鐵礦物的方式從液相轉移到固相.
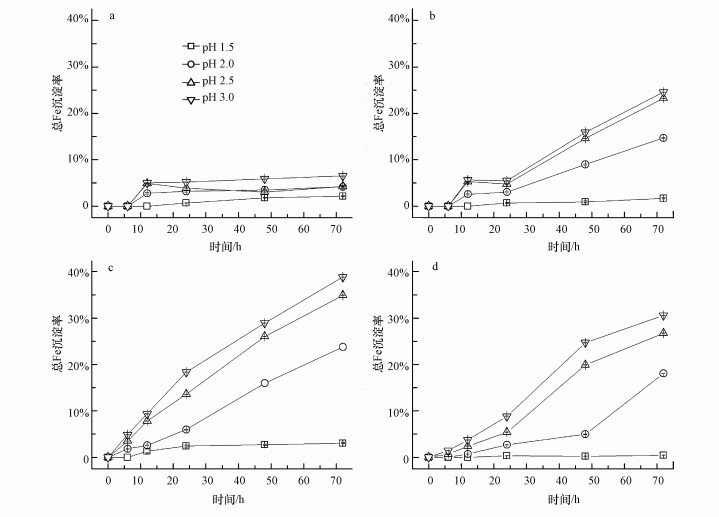
圖 2溶液起始pH和反應溫度對Fe3+水解沉淀的影響(a.8 ℃;b.18 ℃;c.28 ℃;d.38 ℃)
當反應溫度為8 ℃時(圖 2a), 通過觀察發現, 只有pH=3.0處理中出現渾濁, 有少量沉淀生成, 計算總Fe沉淀率為6.50%;而其它處理中則液體澄清, 瓶壁干凈, 沒有明顯的固相生成.究其原因有兩個:一是低溫不利于細菌氧化Fe2+(圖 1a和表 1), 從而導致體系中的Fe3+濃度低, 繼而不利于次生礦物的形成;另外一個就是次生礦物的形成是一個吸熱反應, 所以溫度低不利于Fe3+水解反應的進行.當溫度提高到18 ℃時(圖 2b), 除了起始pH=1.5處理外, 其它反應體系中均有沉淀生成, 且反應24 h后總Fe沉淀率呈直線上升趨勢, 結合表 1可以推測, Fe2+氧化速度的加快(24~48 h)促進體系Fe3+濃度的提高有利于次生礦物的生成.總體來說, 起始pH越高, 越有利于除去溶液中的可溶性鐵.當溫度提高到28 ℃時(圖 2c), 除pH=1.5處理外, 所有處理中總Fe沉淀率從反應啟動時就開始直線上升, 生成大量次生鐵礦物, 反應72 h后, pH=2.0、2.5、3.0時總Fe沉淀率分別達到23.75%、34.92%、38.85%.當溫度為38 ℃時(圖 2d), 較高pH處理也能保證一定的總Fe沉淀率.通過與18 ℃條件下的結果相比較發現, 雖然溫度升高不利于A.ferrooxidans對Fe2+充分氧化, 但卻能夠顯著促進次生鐵礦物的生成.說明高溫促進了Fe3+的水解, 吸熱效應促使次生鐵礦物的形成反應平衡向右移動.
3.3 溶液溫度和pH對次生鐵礦物顏色和重量的影響
表 2是不同處理培養72 h后收集的次生鐵礦物的顏色和質量.采用土壤標準比色卡對礦物顏色進行比對, 發現礦物的顏色變化具有一定的規律性, 大致如下:在溫度相同的情況下, 隨著起始pH的升高, 礦物的顏色由淺入深, 由黃色向紅色轉變.如在18 ℃條件下, 隨著溶液的起始pH從2.0升到3.0, 礦物的顏色逐漸由黃色, 經黃橙色過渡到淡紅棕色.在起始pH相同的情況下, 隨著反應溫度的升高, 礦物的顏色由深變淺.
表 2 不同pH和溫度處理下生成礦物的顏色和質量
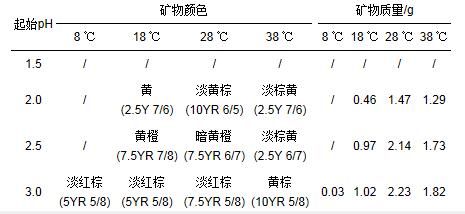
不同反應條件下, 生物成因次生礦物量具有明顯差異.起始pH=1.5時, 不同溫度處理均未發現有礦物生成, 起始pH越高, 收集礦物量越多.溫度為8 ℃時, 只有pH=3.0處理中有0.03 g礦物生成.當溫度升高到18 ℃時, 礦物的形成量明顯增多, 相對于8 ℃而言, 18 ℃下在pH=2.0時就發現有礦物形成.當溫度為28 ℃時, 礦物生成量明顯增多, 如pH=3.0處理礦物量達到2.23 g.當溫度為38 ℃時, 不同pH條件下生成礦物量雖然相對28 ℃有所減少, 但仍遠多于18 ℃處理, 這與圖 2總Fe沉淀率的規律較為一致.
3.4 溶液溫度和pH對次生鐵礦物相的影響及調控
圖 3為改良9K培養基中培養72 h時收集得到的次生鐵礦物XRD譜.顯然, 溫度和起始pH對體系次生鐵礦物的種類都有一定的影響.在18 ℃環境下, 起始pH=2.5和pH=3.0處理收集的次生鐵礦物應為同一物質, 根據其衍射峰位置及相對強度, 分析礦物為一種無定型的施威特曼石.而起始pH=2.0時, 次生礦物開始出現微弱的黃鐵礬衍射峰.柏雙友等研究結果表明, Fe3+供應速度的提高是促進次生礦物相向黃鐵礬轉變的主要原因, 在相同條件下, 80 mmol·L-1 Fe2+時產物為純凈的施氏礦物, 而80 mmol·L-1 Fe2++10 mmol·L-1 Fe3+時主要產物為黃鐵礬.而結合圖 1可以發現, pH=2.0時Fe2+氧化速度不及pH=2.5~3.0, 這也間接說明促使黃鐵礬生成的因素不僅僅局限于Fe2+氧化速度, 與體系pH也密切相關.當溫度上升至28 ℃時, 起始pH=3.0時收集到的礦物為單一施威特曼石, 而在pH=2.0~2.5范圍內, pH降低有利于黃鐵礬的生成, 且pH越低, 表征的衍射峰越強, 這與Liao等研究結果一致.此外發現, 不同pH處理在38 ℃時獲得礦物相均為無定型的施威特曼石, 結合圖 1可以判斷, 較低的Fe3+供應速度是導致此溫度下次生礦物相為施威特曼石的主要原因.Kupka等研究表明, 在5 ℃環境下培養17 d后生成的礦物以施威特曼石為主, 并含有少量的黃鉀鐵礬, 而在30 ℃時則相反.因本研究培養時間只有3 d, 故在低溫時并未收集到任何礦物相的次生產物, 但從溫度18~28 ℃、pH=2.0~2.5時的培養結果來看, 與上述學者結論并不矛盾.Wang等報道, 溫度的升高有利于施威特曼石向黃鉀鐵礬轉變, 這在圖 3中也有所體現, 但前提是溫度不能過于極端, 且要保證培養體系起始pH在一定范圍內.
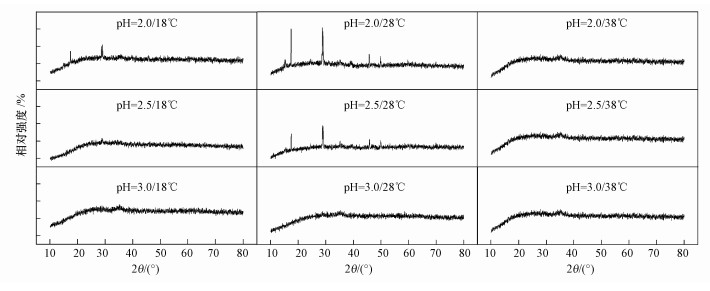
圖 3不同處理生物成因次生鐵礦物的XRD圖譜
在適宜環境條件下, A.ferrooxidans氧化Fe2+成Fe3+后, 體系成礦主要反應方程式如下:
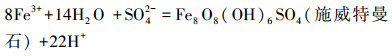
(4)
當體系存在一定濃度一價陽離子時(M+=Na+、K+、NH4+), Fe3+會水解生成黃鐵礬:
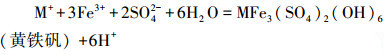
(5)
理論上, 次生礦物完全按反應式(4) 或(5)單獨進行時, 單位Fe3+所合成純黃鐵礬質量應為純施威特曼石的1.5倍以上.在知曉溫度和起始pH對次生鐵礦物相影響的基礎上, 結合表 2和圖 3發現, 18~28 ℃溫度下獲得施威特曼石和黃鉀鐵礬的混合物質量均小于純施威特曼石, 與理論結果“相悖”, 這主要受體系起始pH的影響.因為施威特曼石為典型的球形海膽結構, 且具有較高的比表面積, 易于溶質擴散和礦物溶解.劉奮武等在酸性環境下考察了施威特曼石的穩定性, 結果表明, 在15 ℃搖床中振蕩72 h, pH=3.0體系中施威特曼石溶解率只有3.34%, 而當pH下調至2.0時, 相同時間內溶解率達到61.46%.這也對本研究結果進行了佐證, 且由反應式(4)和(5) 可知, Fe3+水解成礦是產酸過程, 隨著反應的不斷進行, 體系pH相對起始值會更低, 更易提高施威特曼石溶解程度.依此可以推斷, 要使得施威特曼石大量合成和總Fe沉淀率提高, 對反應體系溫度和pH的適當調控至關重要.
結合前面的試驗結果, 對不同pH和溫度條件下Fe2+氧化和Fe3+水解成礦的若干規律及其控制條件進行了總結:以提高溶液Fe3+濃度為目的:在涉及A.ferrooxidans工程應用中, 如煙氣脫硫, 次生礦物的生成會減少反應器中作為氧化劑的Fe3+的濃度, 且其在管道、閥門等位置的沉積還會影響反應器的正常運轉.所以, 若要確保溶液具有較高的Fe3+濃度且防止次生礦物形成, 則最佳控制反應條件為溫度28 ℃和起始pH=1.5, 此時48 h內Fe2+的平均氧化速率為187 mg·L-1·h-1, TFe沉淀率只有2.69%.以提高施氏礦物生物合成率為目的:施氏礦物具有納米級粒度和不規則孔道結構, 具有較大比表面積且富含羥基、硫酸根等基團, 對重(類)金屬具有很強的吸附能力和共沉淀作用, 在重金屬廢水領域具有潛在的應用價值.研究結果表明, 若要促使Fe2+快速氧化同時大量合成施氏礦物, 最佳控制條件為28 ℃和pH=3.0, 此時24 h內Fe2+的平均氧化速率為357 mg·L-1·h-1, 72 h內TFe沉淀率高達38.85%.以提高黃鐵礬生物合成率為目的:黃鐵礬具有不溶解于稀酸, 易于沉淀、洗滌和過濾等優點, 是稀有昂貴的赭黃色無機顏料.因此, 若從無機顏料的角度出發, 以促進次生鐵礦物向黃鐵礬轉換為目的, 則控制反應溫度28 ℃和pH=2.0~2.5為宜
4 結論
1) 溫度和pH均影響Fe2+生物氧化和Fe3+水解成礦.A.ferrooxidans在28 ℃時生長最為適宜, 18 ℃次之, 而10 ℃和38 ℃則都不利于細菌生長繁殖, 導致Fe2+氧化速度明顯變慢.pH=2.0~3.0對A.ferrooxidans的氧化活性沒有明顯影響, 而pH=1.5對其有顯著的抑制作用.
2) 在適宜溫度下, 體系初始pH會影響生物成因次生礦物的產量及礦物相.在改良9K培養基中, 以促進次生鐵礦物向黃鐵礬轉換為目的, 則控制反應溫度28 ℃、pH=2.0~2.5為宜.若要保證Fe2+快速氧化同時提高總Fe沉淀率和施氏礦物的大量生成, 最佳控制條件為28 ℃、pH=3.0.這對去除酸性礦山廢水中可溶性Fe、SO42-及有效調控次生礦物的形成具有潛在意義.
上一篇:平菇菌糠如何吸附廢水中銅離子
下一篇:如何提高絮凝沉降法處理有色廢水的效率